Dossier rédigé par Hélène Joubert, avec le Dr Thierry Perez, pneumologue, service de Pneumologie et Immuno-Allergologie (Institut Cœur Poumon, CHU de Lille) et le Dr Bruno Stach, pneumologue (Valencienne).
INTRODUCTION
Examen de première intention des explorations fonctionnelles respiratoires (EFR), la spirométrie est l’exploration de référence pour détecter un trouble ventilatoire obstructif (TVO). Elle est notamment indispensable au diagnostic d’asthme et de bronchopneumopathie chronique obstructive (BPCO) ainsi qu’au suivi de ces pathologies.
Avec l’emploi de spiromètres miniaturisés permettant de s’affranchir des cabines de pléthysmographie, sa réalisation est devenue possible en cabinet de ville, en particulier chez le généraliste.
Pour autant, cela n’a pas permis de démocratiser largement l’examen. Entre 2010 et 2018, 7,2 % des spirométries effectuées en France chez les patients de 40-75 ans l’ont été par des généralistes exerçant en cabinet libéral (1). Bien que davantage de généralistes réalisent des spirométries ces dernières années, ce nombre reste largement insuffisant pour un repérage et un suivi optimal des pathologies respiratoires. Dans sa fiche pertinence de soins dédiée à la BPCO (2), La HAS réaffirme pourtant le rôle du généraliste dans la réalisation des spirométries. Mais plusieurs freins ont été identifiés par la profession qui pointe notamment, le caractère chronophage de l’examen, la nécessité de le pratiquer régulièrement, le coût des consommables mais aussi l’obligation de formation théorique et pratique de six heures*. Et actuellement, une part des généralistes opte en faveur de la délégation de tâches à une infirmière Asalée ou une assistante médicale au sein de leur CPTS ou MSP. Des protocoles de coopération entre médecin délégant et IDE ou kinésithérapeute délégué à la réalisation de l’examen sont d'ailleurs en cours d’évaluation.
Alors que la BPCO reste largement sous-diagnostiquée, de nouvelles règles de cotations plus favorables sont récemment entrées en vigueur pour les spirométries effectuées dans le cadre du repérage de la BPCO (voir ci-dessous) et la communauté pneumologique se mobilise pour faire bouger les lignes.
Après avoir rappelé les enjeux et les principales indications de la spirométrie en soins primaires, cet article revient les fondamentaux pour la bonne réalisation et l’interprétation de la spirométrie en particulier dans la BPCO.
LES INFORMATIONS FOURNIES PAR LA SPIROMÉTRIE
La spirométrie fait partie des explorations fonctionnelles respiratoires qui permettent la mesure des volumes pulmonaires et des débits bronchiques. Les EFR comportent également la pléthysmographie, la mesure de la diffusion du monoxyde de carbone (DLCO) et les gaz du sang artériel.
La spirométrie mesure de façon non invasive des volumes et des débits ventilatoires dynamiques, obtenus lors de manœuvres respiratoires standardisées (inspiration maximale, expiration forcée ou lente). Elle fournit ainsi plusieurs informations : elle mesure directement la capacité vitale lente (CVL), le volume expiratoire maximal en une seconde (VEMS), la capacité vitale forcée (CVF), les débits expiratoires (dont le débit expiratoire de pointe -DEP), et permet l’obtention des courbes débit-volume. Elle fournit également des paramètres calculés tels que le rapport VEMS/CVF.
La spirométrie est l’examen de référence pour diagnostiquer et évaluer un trouble ventilatoire obstructif (TVO). En revanche, elle ne mesure pas le volume résiduel ni la capacité pulmonaire totale et ne peut donc que suggérer un trouble ventilatoire restrictif, sans le confirmer.
QUELLE PLACE EN MÉDECINE GÉNÉRALE ?
> Les enjeux
En médecine générale, l’objectif de la spirométrie est de détecter, diagnostiquer et suivre l’évolution des troubles ventilatoires obstructifs (asthme et BPCO au premier plan). En augmentant le recours à la spirométrie en soins primaires, l’enjeu est à la fois de :
• Réduire le sous-diagnostic des TVO et notamment de la BPCO.
En France, la prévalence de la BPCO est estimée à environ trois millions de patients, avec un taux de détection aux alentours de 20 % selon la HAS (3). Ce sous-diagnostic persiste malgré la disponibilité de la spirométrie en médecine générale, favorisé également par un manque de recherche active des symptômes classiques de la BPCO (dyspnée, toux, expectoration, exacerbations…).
Par ailleurs, dans la BPCO, prescrire un traitement inhalé sans effectuer un test diagnostique par spirométrie dans des délais rapides peut exposer le patient à un traitement inefficace ou inutile, avec son risque d’effets indésirables et son coût, et retarder le diagnostic formel de la pathologie.
• Mieux étayer (ou écarter) les diagnostics positifs et les prescriptions notamment dans l’asthme.
Dans l’asthme, nombreux sont les diagnostics posés sans spirométrie, ou du moins sans test de réversibilité. Dans une étude menée en Allemagne (4), seulement 7 % des patients asthmatiques avaient eu une spirométrie pendant la période d’étude.
En cas d’asthme, évaluer la fonction respiratoire sert à quantifier le niveau d’obstruction bronchique, tester sa réversibilité, mais aussi surveiller la progression de la maladie, ajuster le traitement de fond et de secours et prévenir la survenue d’exacerbations. Les recommandations de la Global Initiative for Asthma (GINA)(5) font de la spirométrie (incluant le test de réversibilité) un élément clé du diagnostic et du suivi de l’asthme. Comme la HAS, la GINA précise que le diagnostic repose sur l’évaluation des symptômes clinique et des preuves objectives de limitation/réversibilité des débits.
> Les indications « hors pneumologie »
En soins primaires, il est recommandé de pratiquer une spirométrie avec test de réversibilité au bronchodilatateur chez un patient à l’état stable, en cas de :
• Suspicion de BPCO (associé à l’auto-questionnaire HAS, BPCO) fondée sur des signes fonctionnels chez un patient à risque
- âge > 40 ans ;
-et tabagisme (présent ou passé) à au moins 10 paquet-années et/ou exposition professionnelle (empoussiérage) et/ou domestique (combustion de biomasse), infections respiratoires de l’enfance ;
- et symptômes ou signes respiratoires (toux, expectoration, dyspnée, « bronchites à répétition », râles bronchiques).
• Suspicion d’asthme : dyspnée avec sibilants, toux, expectoration, « bronchites à répétition », sibilants à l’auscultation, variabilité importante des symptômes.
• Suivi de BPCO ou d’asthme (associé au questionnaire COPD Assessment TEST CAT, ou au score de contrôle de l’asthme ACT ou ACQ).
La spirométrie est utile pour le suivi du patient atteint de BPCO et d’asthme. Elle permet d’évaluer l’évolution du VEMS au cours du temps, d’objectiver le degré d’obstruction bronchique et de surveiller la réponse aux traitements bronchodilatateurs.
Elle participe aussi à la classification de la sévérité spirométrique de la maladie selon les recommandations.
Le suivi spirométrique sera réalisé :
- de façon systématique (annuel ou plus fréquent en cas d’asthme ou BPCO sévère). Lors du suivi, il est en effet recommandé que les patients BPCO bénéficient d’une spirométrie annuelle, ce qui n’est le cas que de 34 % d’entre eux selon la HAS ;
- en cas de dégradation symptomatique ;
- en post-exacerbation.
> Les contre-indications
• Il n’y a plus de contre-indications absolues à la spirométrie mais uniquement des contre-indications relatives :
- sur le plan cardiaque : HTA sévère non contrôlée, infarctus du myocarde (IDM) < 7j ; angor instable ;
- sur le plan respiratoire : embolie pulmonaire récente (< 2 semaines), hémoptysie, pneumothorax (< 2 mois) ; tuberculose active ou infection respiratoire active ;
- chirurgie ophtalmologique ou ORL récente ;
- sur le plan neurologique : hypertension intracrânienne, anévrisme cérébral.
RÉALISATION DE LA SPIROMÉTRIE
> Un examen en 3 étapes
La réalisation de la spirométrie comprend 3 étapes
• Mesure de la capacité vitale lente (CVL) : volume d’air expiré lentement, depuis une inspiration maximale jusqu’à une expiration complète, sans effort forcé. Elle indique le volume d’air maximal mobilisable entre une inspiration complète et une expiration lente maximale. La manœuvre de CVL permet de mesurer les volumes mobilisables (capacité inspiratoire, volume de réserve inspiratoire et volume de réserve expiratoire).
• Mesure de la capacité vitale forcée (CVF) qui quantifie les volumes mobilisables au cours d’une expiration forcée. Elle permet le tracé automatique de la courbe débit/volume (et de la courbe volume/temps), représentation graphique reliant le débit expiratoire/inspiratoire au volume pulmonaire lors d’une manœuvre forcée.
Plusieurs données sont obtenues, dont la valeur de la CVF elle-même, le VEMS, les débits expiratoires instantanés et maximaux (DEP), ainsi que les valeurs calculées incluant le rapport VEMS/CVF.
• En cas de TVO, on procède dans un second temps (au cours du même examen) à un test de réversibilité, seul moyen de distinguer entre un TVO réversible (comme l’asthme) d’un TVO peu ou pas réversible (comme la BPCO), voire mixte.
Le patient inhale 400 µg de salbutamol en aérosol-doseur pressurisé (Ventoline), en 4 bouffées espacées de 30 secondes et administrées par l’intermédiaire d’une chambre d’inhalation. Puis 10 à 15 minutes après l’inhalation, de nouvelles courbes de CVF sont réalisées.
Dans le cadre d’une spirométrie de repérage en médecine générale, ce test de bronchodilatation n’est pas toujours possible et sera, dans ce cas, réalisé par le pneumologue.
> En pratique
• En prétest, le patient doit s’abstenir de consommer de l’alcool dans les 4 heures précédant l’examen, de manger dans les 2 heures, de fumer dans l’heure et d’effectuer un effort physique dans les 30 minutes. Il doit également éviter de porter des vêtements qui limitent l’expansion thoracique ou abdominale.
• Pour la réalisation de la spirométrie, le patient est en position assise ou debout, le dos bien droit, sans exagérer la flexion ou l’extension du rachis cervical. Le patient doit être détendu ; le professionnel de santé prend le temps d’expliquer en détail les différentes manœuvres à effectuer durant l’examen. Un pince-nez est appliqué pour éviter toute fuite d’air par les narines. Le patient referme les lèvres autour de l’embout buccal (étanchéité souple).
CVL : le patient inspire lentement jusqu’à atteindre la capacité pulmonaire totale puis il expire aussi lentement et complètement que possible, sans effort brusque, jusqu’à ce que le volume expiré soit maximal.
CVF : l’examen débute par une inspiration maximale (inspiration complète et rapide) suivie immédiatement d’une expiration forcée (pause brève avant la manœuvre expiratoire inférieure à 1 seconde), la plus intense dès le début et la plus prolongée possible.
Absence de toux (notamment au début) et absence de fermeture de la glotte.
Au minimum trois mesures doivent être réalisées, qui doivent être superposables.
Tout au long de l’examen, le rôle du praticien est capital. Son accompagnement vocal et gestuel motive le patient et favorise son implication, ce qui est indispensable pour obtenir des tracés fiables et exploitables.
Les points critiques à obtenir sont une inspiration complète, un bon début de manœuvre et surtout une fin d’expiration correcte.
Un effort expiratoire insuffisant peut donner des résultats faussement augmentés du VEMS et des débits expiratoires (en diminuant la compression dynamique des voies aériennes), d’où l’importance d’une implication maximale du patient. Une expiration incomplète surestime le rapport VEMS/CVF et peut entraîner un faux négatif.
L’INTERPRÉTATION DE LA SPIROMÉTRIE
>Les prérequis
Avant d’interpréter les résultats d’une spirométrie, il faudra :
• Évaluer l’acceptabilité des courbes :
– absence d’artefacts de toux ou de fermeture de glotte ;
– bon départ : DEP précoce, c’est-à-dire survenant dans un délai < 120 ms après le début de l’expiration ou volume extrapolé du VEMS < 0,15 L ou 5 % de la CVF (ce volume calculé par le logiciel permet de détecter un début d’expiration trop lent) ;
– critères d’expiration complète : durée expiration ≥ 15 secondes ou surtout plateau sur la courbe temps volume ou sujet incapable de poursuivre l’expiration ;
– effort suffisant et reproductible ; (voir ci-dessous).
Si ces critères ne sont pas remplis, les résultats ne doivent pas être interprétés ou seulement avec réserve.
Cela concerne 5 à 10 % des courbes, même dans les laboratoires d’explorations fonctionnelles.
• Évaluer la reproductibilité des résultats
Celle-ci doit être vérifiée sur trois manœuvres techniquement satisfaisantes : pour le VEMS et la CVF, l’écart entre les deux meilleures valeurs doit être inférieur à 150 mL. Si ce critère n’est pas atteint, il faut poursuivre les essais jusqu’à obtention de la reproductibilité, avec un maximum de 8 manœuvres ou jusqu’à ce que le patient soit incapable de continuer. Les trois meilleurs tests doivent être sauvegardés. À partir des trois meilleures courbes reproductibles validées, le spiromètre retient automatiquement la meilleure CVF et le meilleur VEMS, même si elles proviennent de courbes différentes ; la courbe sélectionnée est celle présentant la plus grande somme VEMS + CVF.
> Interpréter les résultats
Lors de la réalisation de l’examen, les résultats apparaissent sous la forme d’une courbe débit/volume qui facilite leur interprétation. Ces données sont aussi présentées numériquement.
Le rapport VEMS/CVF s’exprime en pourcentage et en pourcent de la théorique (selon les informations saisies par le professionnel, le logiciel dispose de « valeurs de référence » propres à chaque individu, établies en fonction du poids, de la taille et de l’origine ethnique).
• En cas de TVO, il existe une réduction des débits par rapport aux volumes, donc par définition le rapport VEMS /CVF est diminué.
Un rapport VEMS/CVF < 70 % après un bronchodilatateur (test de réversibilité) pose le diagnostic de BPCO.
Cependant, ce critère peut conduire à un sous-diagnostic de l’obstruction bronchique chez les patients de moins de 50 ans, et surtout à un surdiagnostic chez les patients plus âgés. L’alternative est une définition de l’obstruction bronchique fondée sur un VEMS/CVF < la limite inférieure de la normale (LIN) qui représente la valeur du 5e percentile dans une population de référence jugée exempte de maladie.
Le TVO de la BPCO persiste après bronchodilatateurs, ce qui n’est pas le cas de l’asthme, où l’obstruction bronchique est en général réversible.
• Un TVO est dit « réversible » si, lors de la réalisation de nouvelles courbes post-bronchodilatation, on observe une amélioration du VEMS d’au moins 12 % et au moins 200 ml par rapport à la valeur initiale (réversibilité significative). Dans ce cas :
- si VEMS et VEMS/CVF post-bronchodilatateur normaux → TVO complètement réversible ;
- si VEMS post-bronchodilatateur < normale → TVO partiellement réversible.
Si la réversibilité n’est jamais totale dans la BPCO, elle peut toutefois être partielle. Le diagnostic de BPCO peut être retenu lorsque les critères de réversibilité sont présents mais que le rapport VEMS/CVF reste abaissé et que le VEMS ou la CVF ne sont pas normalisés.
En l’absence d’amélioration significative en post-bronchodilatateur, le TVO est non réversible (BPCO). À noter, la réversibilité peut varier d’un jour à l’autre chez le patient BPCO.
Une réversibilité marquée doit faire suspecter un asthme, (diagnostic différentiel ou associé), mais aucun seuil précis ne distingue clairement BPCO et asthme (certaines recommandations proposent le seuil de 400 mL).
• Le VEMS est le principal indicateur de la sévérité du TVO, avec une valeur pronostique majeure. Il guide également en partie les choix thérapeutiques et leur évaluation.
• Un TVR peut être suggéré par une capacité vitale forcée diminuée avec un rapport VEMS/CVF normal ou augmenté. Le diagnostic repose sur la mesure des volumes pulmonaires statiques, en particulier la capacité pulmonaire totale (pléthysmographie ou dilution des gaz).
QUAND ADRESSER AU PNEUMOLOGUE ?
En dehors d’un résultat négatif chez un patient asymptomatique tout résultat anormal de la spirométrie doit conduire à un bilan pneumologique.
En particulier :
• En cas d’anomalies à la spirométrie évoquant un TVO pour confirmation diagnostique (BPCO versus asthme, association asthme-BPCO, dilatations des bronches, autres causes).
Dans ce cas, un traitement de 1re ligne conformément aux recommandations en vigueur doit être instauré et un sevrage tabagique proposé.
En parallèle, le patient doit aussi être intégré dans un parcours de soins coordonné. Après bilan approfondi par un pneumologue (exploration de diagnostics différentiels d’obstruction bronchique, vaccinations, etc.) et stabilisation (adaptation thérapeutique), le patient est suivi par son médecin traitant dans le cadre d’une collaboration pluriprofessionnelle.
• En cas de suspicion de TVR.
• Si la spirométrie est normale mais que le patient est symptomatique. En effet, si chez un patient asymptomatique, une spirométrie normale suffit généralement à écarter une atteinte respiratoire, chez un patient présentant des symptômes respiratoires, tels qu’une plainte d’essoufflement au repos ou à l’effort, un bilan spécialisé doit être réalisé, même si la spirométrie est normale. La persistance d’une dyspnée doit en effet conduire à rechercher d’autres causes, comme une pathologie interstitielle débutante ; une hypertension pulmonaire ; un syndrome d’hyperventilation ; une affection cardiaque ; etc.
La spirométrie peut également être normale en période intercritique chez l’asthmatique.
• Lors du suivi spirométrique d’un patient avec pathologie confirmée, en cas de dyspnée ou de handicap disproportionnés ou s’aggravant ; d’exacerbations fréquentes ou sévères ; d’asthme non contrôlé ; de comorbidités avec impact respiratoire (cardiopathie, par exemple).
Cotation de l’acte depuis le 1er janvier 2026
Depuis le 1er janvier 2026, sous réserve que le patient réponde à trois conditions*, le praticien peut cumuler 100 % des honoraires de l'acte de mesure de la capacité vitale lente et de l'expiration forcée, avec enregistrement [Spirométrie standard] (GLQP012)** (sous réserve d’une facturation à tarif opposable) avec ceux de la consultation de référence ou coordonnée à tarif opposable pour les pneumologues et les généralistes, dans le cadre du dépistage de la BPCO. Cela ne s’applique qu’au secteur 1 ou 2 avec OPTAM. Le médecin doit avoir suivi une formation spécifique à la spirométrie. Un seul cumul avec une consultation est facturable par an et par patient.
* Avoir plus de 40 ans, consommer plus de 20 paquets par an et avoir été détecté à risque dans le questionnaire dépistage BPCO de la HAS.
** Le GLQP012 est à 41,87 euros (depuis le 1er janvier 2026) et peut donc s’associer au G (30 euros), soit G + GLQP012 = 71,87 euros. Les pneumologues peuvent aussi associer leur consultation CS +MCS + GLQP012 soit 73,37 euros.
Quel matériel ?
En soins primaires, la spirométrie repose sur l’utilisation de spiromètres électroniques compacts (marqués CE).
Il existe plusieurs types de capteur de débit :
- à turbine de dernière génération (à usage unique ou multiple),
- à ultrasons (à usage unique ou multiple),
- à résistance (pneumotachographe ; à tubes laminaires de type Fleisch ou à grille métallique de type Lilly ou à orifice variable). Ces capteurs qui requièrent un calibrage quotidien sont de moins en moins utilisés en soins primaires.
Compter environ 1 000 à 1 500 euros pour l’achat d’un spiromètre.
À noter que les débitmètres portables type Peak Flow électronique ou minispiromètres mesurent principalement le DEP, le VEMS voire le rapport VEMS/VEM6 (volume expiré en 6 secondes). C’est un outil de dépistage ou de suivi rapide d’un TVO connu tandis que la spirométrie est un examen diagnostic complet.
*L’actualisation de la formation DPC SPLF/FFP/ collège de la médecine générale est prévue au 1er semestre 2026.
Bibliographie :
(1) Chapron A et al. Spirometry practice by French general practitioners between 2010 and 2018 in adults aged 40 to 75 years. npj Prim. Care Respir. Med. 33, 33 (2023). https://doi.org/10.1038/s41533-023-00352-9
(2) HAS. Guide du parcours de soins Bronchopneumopathie chronique obstructive. Novembre 2019
(3) HAS. BPCO : des indicateurs pour améliorer le parcours de soins. Avril 2022
(4) Härtel A, Peters M, Kostev K. Prevalence of Spirometry Testing among Patients with Asthma and COPD in German General Practices. Healthcare. 2022; 10(12):2570. https://doi.org/10.3390/healthcare10122570
(5) Global initiative for asthma. Global Strategy for Asthma anagement and Prevention. Updated 2023.
Liens d’intérêts : Le Dr Bruno Stach déclare n’avoir aucun lien d’intérêts relatif au contenu de cet article.





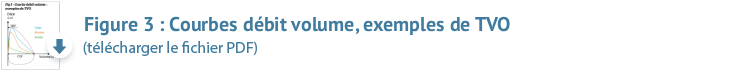
Cas clinique
Le phimosis
En 5 points
L’halitose
Etude & Pratique
Antihypertenseurs en Ehpad, la déprescription en question
En 5 points
L’énurésie